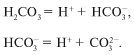Разделы сайта
Выбор редакции:
- День Бородинского сражения
- Что такое научная работа
- Угольная кислота и её соли - получение и применение Химические взаимодействия между электролитами
- Роль водородной связи в процессах ассоциации, растворения и биохимических процессах Внутримолекулярные водородные связи
- Конспект урока на тему: "Степени сравнения имен прилагательных"(6класс) Конспект урока сравнительная степень прилагательных
- Places of Interest in London - Достопримечательности Лондона, устная тема по английскому языку с переводом
- Кладбище кораблей: последняя пристань гигантов (6 фото)
- Презентация по физике на тему "электрический ток в металлах"
- Бонч-бруевич михаил александрович Что создал м а бонч бруевича
- Флавий маврикий тиберий август Ирод, Флавий, Ирод, Флавий, фигуры истории
Реклама
| Электролиты. Угольная кислота и её соли - получение и применение Химические взаимодействия между электролитами |
|
1. ЭЛЕКТРОЛИТЫ 1.1. Электролитическая диссоциация. Степень диссоциации. Сила электролитов Согласно теории электролитической диссоциации, соли, кислоты, гидроксиды, растворяясь в воде, полностью или частично распадаются на самостоятельные частицы – ионы. Процесс распада молекул веществ на ионы под действием полярных молекул растворителя называют электролитической диссоциацией . Вещества, диссоциирующие на ионы в растворах, называют электролитами. В результате раствор приобретает способность проводить электрический ток, т.к. в нем появляются подвижные носители электрического заряда. Согласно этой теории, при растворении в воде электролиты распадаются (диссоциируют) на положительно и отрицательно заряженные ионы. Положительно заряженные ионы называют катионами ; к ним относятся, например, ионы водорода и металлов. Отрицательно заряженные ионы называются анионами ; к ним принадлежат ионы кислотных остатков и гидроксид-ионы. Для количественной характеристики процесса диссоциации введено понятие степени диссоциации. Степенью диссоциации электролита (α) называется отношение числа его молекул, распавшихся в данном растворе на ионы (n ), к общему числу его молекул в растворе (N ), или α = . Степень электролитической диссоциации принято выражать либо в долях единицы, либо в процентах. Электролиты со степенью диссоциации больше 0,3 (30%) обычно называют сильными, со степенью диссоциации от 0,03 (3%) до 0,3 (30%)-средними, менее 0,03 (3%)-слабыми электролитами. Так, для 0,1 M раствора CH 3 COOH α = 0,013 (или 1,3 %). Следовательно, уксусная кислота является слабым электролитом. Степень диссоциации показывает, какая часть растворенных молекул вещества распалась на ионы. Степень электролитической диссоциации электролита в водных растворах зависит от природы электролита, его концентрации и температуры. По своей природе электролиты можно условно разделить на две большие группы: сильные и слабые . Сильные электролиты диссоциируют практически полностью (α = 1). К сильным электролитам относятся: 1) кислоты (H 2 SO 4 , HCl , HNO 3 , HBr , HI , HClO 4 , H М nO 4 ); 2) основания – гидроксиды металлов первой группы главной подгруппы (щелочи) – LiOH , NaOH , KOH , RbOH , CsOH , а также гидроксиды щелочноземельных металлов – Ba (OH ) 2 , Ca (OH ) 2 , Sr (OH ) 2 ;. 3) соли, растворимые в воде (см. таблицу растворимости). Слабые электролиты диссоциируют на ионы в очень малой степени, в растворах они находятся, в основном в недиссоциированном состоянии (в молекулярной форме). Для слабых электролитов устанавливается равновесие между недиссоциированными молекулами и ионами. К слабым электролитам относятся: 1) неорганические кислоты (H 2 CO 3 , H 2 S , HNO 2 , H 2 SO 3 , HCN , H 3 PO 4 , H 2 SiO 3 , HCNS , HСlO и др.); 2) вода (H 2 O ); 3) гидроксид аммония (NH 4 OH ); 4) большинство органических кислот (например, уксусная CH 3 COOH, муравьиная HCOOH); 5) нерастворимые и малорастворимые соли и гидроксиды некоторых металлов (см. таблицу растворимости). Процесс электролитической диссоциации изображают, пользуясь химическими уравнениями. Например, диссоциация соляной кислоты (НС l ) записывается следующим образом: HCl → H + + Cl – . Основания диссоциируют с образованием катионов металла и гидроксид-ионов. Например, диссоциация КОН КОН → К + + ОН – . Многоосновные кислоты, а также основания многовалентных металлов диссоциируют ступенчато. Например, H 2 CO 3 H + + HCO 3 – , HCO 3 – H + + CO 3 2– . Первое равновесие – диссоциация по первой ступени – характеризуется константой Для диссоциации по второй ступени: В случае угольной кислоты константы диссоциации имеют следующие значения: K I = 4,3 × 10 –7 , K II = 5,6 × 10 –11 . Для ступенчатой диссоциации всегда K I >K II >K III > ... , т.к. энергия, которую необходимо затратить для отрыва иона, минимальна при отрыве его от нейтральной молекулы. Средние (нормальные) соли, растворимые в воде, диссоциируют с образованием положительно заряженных ионов металла и отрицательно заряженных ионов кислотного остатка Ca(NO 3) 2 → Ca 2+ + 2NO 3 – Al 2 (SO 4) 3 → 2Al 3+ +3SO 4 2– . Кислые соли (гидросоли) – электролиты, содержащие в анионе водород, способный отщепляться в виде иона водорода Н + . Кислые соли рассматривают как продукт, получающийся из многоосновных кислот, в которых не все атомы водорода замещены на металл. Диссоциация кислых солей происходит по ступеням, например: KHCO 3 → K + + HCO 3 – (первая ступень) , , 21 , , , § 6.3. Сильные и слабые электролиты
В предыдущем разделе мы обсуждали поведение в
водных растворах некоторых солей и органических
веществ, полностью распадающихся на ионы в
водном растворе.
Водные растворы гидроксидов лития (LiOH), натрия
(NаОН), калия (КОН), бария (Ва(ОН) 2), кальция
(Са(ОН) 2) и других металлов имеют одинаковый
неприятный горько-мыльный вкус и вызывают на
коже рук ощущение скольжения. По-видимому, за это
свойство ответственны гидроксид-ионы ОН – ,
входящие в состав таких соединений. Zn + 2НСl = ZnСl 2 + Н2, а ионы водорода: Zn + 2H + = Zn 2+ + Н 2 , и образуются газообразный водород и ионы цинка. Сопоставляя эти сведения с
электропроводностью водных растворов кислот,
гидроксидов и солей и с рядом других положений,
С.А.Аррениус в 1887 г. выдвинул гипотезу
электролитической диссоциации, согласно которой
молекулы кислот, гидроксидов и солей при
растворении их в воде диссоциируют на ионы. НNO 3 = Н + + . Электролитическая диссоциация
–
полный или частичный распад соединения при его
растворении в воде на ионы в результате
взаимодействия с молекулой воды (или другого
растворителя). HCl – HBr – HI.
Сила однотипных кислородных кислот изменяется
в противоположном направлении, например йодная
кислота НIО 4 слабее хлорной кислоты НСlО 4 .
2 . Гидроксиды элементов главных подгрупп I и II групп периодической системы: LiОН, NaОН, КОН, Са(ОН) 2 и др. При переходе вниз по подгруппе по мере усиления металлических свойств элемента сила гидроксидов возрастает. Растворимые гидроксиды главной подгруппы I группы элементов относят к щелочам.
Гидроксид кальция Са(ОН) 2 как сильный электролит диссоциирует в одну ступень: Са(ОН) 2 = Са 2+ + 2ОН – . 3 . Почти все соли. Соль, если это сильный электролит, диссоциирует в одну ступень, например хлорид железа: FeCl 3 = Fe 3+ + 3Cl – . В случае водных растворов к слабым электролитам ( < 3%) относят перечисленные ниже соединения. 1 . Вода H 2 O – важнейший электролит. 2
. Некоторые неорганические и почти
все органические кислоты: H 2 S
(сероводородная), H 2 SO 3 (сернистая), H 2 CO 3
(угольная), HCN (циановодородная), Н 3 РО 4
(фосфорная, ортофосфорная), H 2 SiO 3
(кремниевая), H 3 BO 3 (борная, ортоборная),
СН 3 СООН (уксусная) и др.
Диссоциация слабой угольной кислоты проходит в
две ступени. Образующийся гидрокарбонат-ион также ведет себя
как слабый электролит.
В водном растворе диссоциация проходит
практически только по первой ступени. Как
сместить равновесие в сторону образования ионов
Fe 3+ ?
NH 4 OH = + ОН – . 5 . Некоторые соли: хлорид цинка ZnCl 2 , тиоцианат железа Fe(NСS) 3 , цианид ртути Hg(CN) 2 и др. Эти соли диссоциируют ступенчато. К электролитам средней силы некоторые относят фосфорную кислоту Н 3 РО 4 . Мы будем считать фосфорную кислоту слабым электролитом и записывать три ступени ее диссоциации. Серная кислота в концентрированных растворах ведет себя как электролит средней силы, а в очень концентрированных растворах – как слабый электролит. Мы далее будем считать серную кислоту сильным электролитом и записывать уравнение ее диссоциации в одну ступень. Новости и события в условиях, при которых она раньше не работала, говорит Константинос Герасопулос, старший научный сотрудник APL, который ведет исследования. Увеличив концентрацию солей лития и смешивания электролита с полимером-материалом, напоминающим очень мягкий... По данным исследований, проведенных Университетом Шеффилда, брошенные символы наступившего праздника можно уберечь от свалки и превратить в краски и пищевые подсластители. Сотни тысяч... На череповецком комплексе АО «Апатит», входящем в состав группы «ФосАгро», в торжественной обстановке дали старт пусконаладочным работам на новом производстве сульфата аммония. Установка произво... внутренних коротких замыканий, которые могут воспламенять жидкие электролиты , что может приводить к взрывам и пожарам. Инженеры из Университета Иллинойса разработали твердый электролит на основе полимеров, который может самовосстановиться после повреждения. Также... Эксперты Роскачества провели испытания искусственных елей, чтобы ответить на вопросы покупателей, связанные с главным новогодним символом. На законодательном уровне требования к искусственным ел... Новое исследование Института технологий Массачусетса посвящено противоположной роли природного газа в борьбе с изменением климата, являющегося мостом к уменьшению выбросов в будущем, но также вн... Информация Ученые создали “неубиваемую” батарею Каталог организаций и предприятий Торговая фирма, специализирующаяся на купле-продаже технической химии: 1. Кислота соляная 2. Кислота серная 3. Кислота ортофосфорная 4. Кислота азотная 5. Этиленгликоль 6. Натр едкий 7. Перекись водор... Мы самый сильный трейдер в Волгоградской области. Мы самый сильный трейдер в Волгоградской области. Мы самый сильный трейдер в Волгоградской области. В 2007 ж/д потребление металлопроката составило примерно 13367т. Предложения на покупку и продажу продукции Предлагаем кислоту азотную хч со склада в г. Саратов. Фасовка-канистры по 20 л (28 кг) .Цена 53 руб/кг. Продам промышленную химию и химическое сырьё. Амины, гидроксиды, гликоли, кислоты, ПАВы, пластификаторы, растворители, соли, спирты, эфиры и др. Изопропиловый спирт, Гипохлорит натрия, Глицерин дистил... Реализуем ортофосфорную кислоту для промышленного применения V не менее 73%, So3 не более 3%, As не более 0, 004 % Отгрузка ЖД цистернами. Цена на жд станции покупателя по запросу. 1. КРАТКАЯ ХАРАКТЕРИСТИКА 1.1. ПАЛЬМИТИНОВАЯ КИСЛОТА, ЕЁ СОЛИ И ЭФИРЫ 1.1.1. Пальмитиновая кислота (Цетиловая) 1.1.2. Соли пальмитиновой кислоты (пальмитаты) 1.1.3. Эфиры пальмитиновой кислоты (п... Организация предлагает со склада в г. Саратов кислоту лимонную пищевую производства Китай. Фасовка-мешки по 25 кг. Скидки от объемов, возможна доставка по городу. Адреса складов в г. Саратов: пос. З... Реализация химической продукции: Оксистибата ртути, пироантимоната ртути, Hg2Sb2О7, Осмий - 187 (Osmium), Красная ртуть М-1 (RM-39/39), 2- диметиламино этанол ч, 2-хлорбензонитрил, 3-хлорбензонитрил, ... Отличные проводники электрического тока — золото, медь, железо, алюминий, сплавы. Наряду с ними существует большая группа веществ-неметаллов, расплавы и водные растворы которых тоже обладают свойством проводимости. Это сильные основания, кислоты, некоторые соли, получившие общее название "электролиты". Что такое ионная проводимость? Выясним, какое отношение имеют вещества-электролиты к этому распространенному явлению. Какие частицы переносят заряды?Мир вокруг полон различных проводников, а также изоляторов. Об этих свойствах тел и веществ известно с глубокой древности. Греческий математик Фалес провел опыт с янтарем (на греческом — «электрон»). Потерев его о шелк, ученый наблюдал явление притяжения волос, волокон шерсти. Позже стало известно, что янтарь является изолятором. В этом веществе нет частиц, которые могли бы переносить электрический заряд. Хорошие проводники — металлы. В их составе присутствуют атомы, положительные ионы и свободные, бесконечно малые отрицательные частицы — электроны. Именно они обеспечивают перенос зарядов, когда пропускают ток. Сильные электролиты в сухом виде не содержат свободных частиц. Но при растворении и расплавлении происходит разрушение кристаллической решетки, а также поляризация ковалентной связи. Вода, неэлектролиты и электролиты. Что такое растворение?Отдавая или присоединяя электроны, атомы металлических и неметаллических элементов превращаются в ионы. Между ними в кристаллической решетке существует достаточно прочная связь. Растворение или расплавление ионных соединений, например, хлорида натрия, приводит к ее разрушению. В полярных молекулах нет ни связанных, ни свободных ионов, они возникают при взаимодействии с водой. В 30-х годах XIX века М. Фарадей обнаружил, что растворы некоторых веществ проводят ток. Ученый ввел в науку такие важнейшие понятия:
Есть соединения - сильные электролиты, кристаллические решетки которых полностью разрушаются с освобождением ионов.
Существуют нерастворимые вещества и те, что сохраняются в молекулярном виде, например, сахар, формальдегид. Такие соединения называются неэлектролитами. Для них не характерно образование заряженных частиц. Слабые электролиты (угольная и уксусная кислота, и ряд других веществ) содержат мало ионов. Теория электролитической диссоциацииВ своих работах шведский ученый С. Аррениус (1859-1927) опирался на выводы Фарадея. В дальнейшем уточнили положения его теории русские исследователи И. Каблуков и В. Кистяковский. Они выяснили, что при растворении и расплавлении образуют ионы не все вещества, а только электролиты. Что такое диссоциация по С. Аррениусу? Это и есть разрушение молекул, которое приводит к появлению заряженных частиц в растворах и расплавах. Основные теоретические положения С. Аррениуса:
Показателем вещества (ее часто выражают в процентах) является соотношение числа молекул, распавшихся на ионы, и общего количества частиц в растворе. Электролиты являются сильными, если значение этого показателя свыше 30%, у слабых — менее 3%. Свойства электролитовТеоретические выводы С. Аррениуса дополнили более поздние исследования физико-химических процессов в растворах и расплавах, проведенные русскими учеными. Получили объяснение свойства оснований и кислот. К первым относят соединения, в растворах которых из катионов можно обнаружить только ионы металла, анионами являются частицы OH - . Молекулы кислот распадаются на отрицательные ионы кислотного остатка и протоны водорода (H +). Движение ионов в растворе и расплаве — хаотичное. Рассмотрим результаты опыта, для которого потребуется собрать цепь, включить в нее и обыкновенную лампочку накаливания. Проверим проводимость растворов разных веществ: поваренной соли, уксусной кислоты и сахара (первые два - электролиты). Что такое электрическая цепь? Это источник тока и проводники, соединенные между собой. При замыкании цепи лампочка будет гореть ярче в растворе поваренной соли. Движение ионов приобретает упорядоченность. Анионы направляются к положительному электроду, а катионы — к отрицательному.
В этом процессе в уксусной кислоте участвует небольшое количество заряженных частиц. Сахар не является электролитом, не проводит ток. Между электродами в этом растворе окажется изолирующий слой, лампочка гореть не будет. Химические взаимодействия между электролитамиПри сливании растворов можно наблюдать, как ведут себя электролиты. Что такое ионные уравнения подобных реакций? Рассмотрим на примере химического взаимодействия между и нитратом натрия: 2NaNO 3 + BaCl 2 + = 2NaCl + Ba(NO 3) 2 . Формулы электролитов запишем в ионном виде: 2Na + + 2NO 3- + Ba 2+ + 2Cl - = 2Na + + 2Cl - + Ba 2+ + 2NO 3- . Взятые для реакции вещества - сильные электролиты. В этом случае состав ионов не меняется. Химическое взаимодействие между возможно в трех случаях: 1. Если один из продуктов является нерастворимым веществом. Молекулярное уравнение: Na 2 SO 4 + BaCl 2 = BaSO 4 + 2NaCl. Запишем состав электролитов в виде ионов: 2Na + + SO 4 2- + Ba 2+ + 2Cl - = BaSO 4(белый осадок) + 2Na + 2Cl - . 2. Одно из образовавшихся веществ — газ. 3. Среди продуктов реакции есть слабый электролит.
Вода — один из наиболее слабых электролитовХимически чистая не проводит электрический ток. Но в ее составе есть небольшое количество заряженных частиц. Это протоны Н + и анионы ОН - . Диссоциации подвергается ничтожно малое число молекул воды. Существует величина — ионное произведение воды, которая является постоянной при температуре 25 °C. Она позволяет узнать концентрации Н + и ОН - . Преобладают ионы водорода в растворах кислот, гидроксид-анионов больше в щелочах. В нейтральных — совпадает количество Н + и ОН - . Среду растворов также характеризует водородный показатель (рН). Чем он выше, тем больше присутствует гидроксид-ионов. Среда является нейтральной при интервале рН близком к 6-7. В присутствии ионов Н + и ОН - изменяют свой цвет вещества-индикаторы: лакмус, фенолфталеин, метилоранж и другие. Свойства растворов и расплавов электролитов находят широкое применение в промышленности, технике, сельском хозяйстве и медицине. Научное обоснование заложено в работах ряда выдающихся ученых, объяснивших поведение частиц, из которых состоят соли, кислоты и основания. В их растворах протекают многообразные реакции ионного обмена. Они используются во многих производственных процессах, в электрохимии, гальванике. Процессы в живых существах также происходят между ионами в растворах. Многие неметаллы и металлы, токсичные в виде атомов и молекул, незаменимы в виде заряженных частиц (натрий, калий, магний, хлор, фосфор и другие). Угольная кислота появляется в результате разложения углекислого газа в водной среде. Этим веществом искусственно насыщают минеральные воды. Формула угольной кислоты Н2СО3. Поэтому при открытии бутылки с газированной водой, можно увидеть активные пузырьки. Основное получение угольной кислоты происходит в воде. УравнениеСО2 (г) + Н2О СО2 . Н2О (раствор) Н2СО3 Н+ + HCO3- 2H+ + CO32-. Сама по себе угольная кислота представляет слабое непрочное соединение, которое невозможно выделить в свободном состоянии из воды. Но стоит отметить тот факт, что во время разложения гидрокарбоната аммония, формируются устойчивые соединения угольной кислоты. Такие крепкие химические связи образуются только в период, когда гидрокарбонат аммония вступает в газовую фазу реакции. Вещество является интересным объектом для изучения. Его изучают австралийские ученые уже более 6 лет. В безводном состоянии эта кислота напоминает прозрачные кристаллы, которые имеют высокую стойкость к низким температурам, но при нагревании кристаллы угольной кислоты начинают разлагаться.
Данное вещество считается слабым по своей структуре, но в тоже время, угольная кислота является сильнее борной. Весь секрет заключается в количестве атомов водорода. В составе угольной кислоты имеется два атома водорода, поэтому она считается двухосновной, а борная кислота - одноосновная. Особенности солей угольной кислотыЭта кислота считается двухосновной, поэтому может создавать соли двух видов:
Карбонатами угольной кислоты могут выступать в соединения: Na2СO3,(NH4)2CO3. Они не способны растворятся в водной среде. Кислые соли этого вещества включают в себя: бикарбонаты NaHCO3 , Ca(HCO3)2. Для получения гидрокарбонатов производят реакцию, в которой основными веществами являются: угольная кислота и натрий.
Соли угольной кислоты помогли человечеству в строительстве, медицине и даже кулинарии. Потому что они встречаются в составе:
Гидрокарбонаты и карбонаты кислоты могут вступать в реакции с кислотами, во время этих реакции возможно выделение углекислого газа. Также эти вещества могут быть взаимозаменяемыми, они способны разлагаться под воздействием температуры. Реакции угольной кислоты: 2NaHCO3 → Na2CO3 +H2O +CO2 Химические свойстваДанная кислота по своей структуре способна входить в реакции со многими веществами. Свойства угольной кислоты раскрываются в реакциях:
Na2O + CO2 → Na2CO3 Угольная кислота представляет собой слабый электролит, так как слабая летучая кислота не может выступать в роли мощного электролита в отличие от, например, соляной кислоты. Этот факт можно увидеть в результате добавление лакмуса в раствор угольной кислоты. Изменение цвета будет незначительным. Поэтому можно утверждать, что угольная кислота может поддерживать 1 уровень диссоциации. ПрименениеДанное вещество можно увидеть в составе газированных вод. Но соли угольной кислоты широко применяют:
Отечественный и мировой рынок предлагает в продаже различные препараты и химические вещества, в состав которых входит угольная кислота:
Карбамид используют в качестве удобрения для плодовых и декоративных растений. Его средняя цена составляет 30-40 рублей за 1 кг. Фасуют готовую продукцию в полиэтиленовые пакеты и мешки, весом 1, 5,25,50 кг. Литиевую соль угольной кислоты используют в составе керамических изделий, ситаллов. Этот материал используется для производства камер сгорания для реактивных двигателей, его добавляют в глазури, эмали, грунтовки для различных металлов. Литиевую соль добавляют в грунтовки для обработки алюминия, чугуна и стали. Это химическое вещество добавляют в процессе стекловарения. Стекла, в состав которых была добавлена литиевая соль, имеют повышенную проницаемость светлового потока. Иногда литиевую соль угольной кислоты используют в процессе производства пиротехники. ПроизводителиСредняя цена 1 кг такого вещества в России составляет 3900-4000 рублей. Главным заводом-изготовителем этого вещества считается московский завод ООО Компонент-Реактив. Также литиевую соль угольной кислоты производят в компаниях: ООО КурскХимПром, ООО ВитаХим, ООО Русхим, ЗАО Химпэк. Мел производится для технических и кормовых целей. Средняя цена кормового мела составляет 1800 рублей за 1 тонну. Фасуется в основном по 50 кг, 32 кг. Производители: ООО Меловик, ООО МТ Ресурс, ООО Зооветснаб, ООО Агрохиминвест. Кальцинированная сода применяется для стирки, удаления пятен и отбеливания. Средняя цена на этот продукт на розничном рынке варьируется в пределах 16-30 рублей за 1 кг. Производители: ООО Новэра, ЗАО ХимРеактив, ООО ХимПлюс, ООО СпецБурТехнологии, ООО СпецКомплект и др. |
Популярное:
Картографическая проекция
|
Новое
- Что такое научная работа
- Угольная кислота и её соли - получение и применение Химические взаимодействия между электролитами
- Роль водородной связи в процессах ассоциации, растворения и биохимических процессах Внутримолекулярные водородные связи
- Конспект урока на тему: "Степени сравнения имен прилагательных"(6класс) Конспект урока сравнительная степень прилагательных
- Places of Interest in London - Достопримечательности Лондона, устная тема по английскому языку с переводом
- Кладбище кораблей: последняя пристань гигантов (6 фото)
- Презентация по физике на тему "электрический ток в металлах"
- Бонч-бруевич михаил александрович Что создал м а бонч бруевича
- Флавий маврикий тиберий август Ирод, Флавий, Ирод, Флавий, фигуры истории
- Плиний Младший – краткая биография Историки о письмах плиния младшего